- Parte 1: Movimento Browniano
- Parte 2: Difusão através de uma Membrana Semipermeável
- Parte 3: Osmose e a membrana celular
- Parte 4: Conceção experimental
A membrana celular desempenha o duplo papel de proteger a célula viva, actuando como uma barreira para o mundo exterior, mas, ao mesmo tempo, deve permitir a passagem de alimentos e resíduos para dentro e para fora da célula para que o metabolismo prossiga. Como é que a célula desempenha estes papéis aparentemente paradoxais? Para compreender este processo, é necessário compreender a composição da membrana celular e umafenómeno importante conhecido como difusão.
A difusão é o movimento de uma substância de uma área de alta concentração para uma área de baixa concentração devido ao movimento molecular aleatório. Todos os átomos e moléculas possuem energia cinética, que é a energia do movimento. É esta energia cinética que faz com que cada átomo ou molécula vibre e se mova. (De facto, pode quantificar a energia cinética dos átomos/moléculas de uma substância através deO movimento das partículas devido a esta energia é designado por movimento browniano. À medida que estes átomos/moléculas se chocam uns com os outros, o resultado é o movimento destas partículas de uma área de alta concentração para uma área de baixa concentração. Este A taxa de difusão é influenciada tanto pela temperatura (a rapidez com que as partículas se movem) como pelo tamanho (a dimensão das partículas).
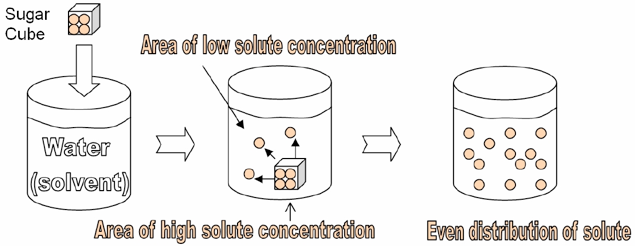
Parte 1: Movimento Browniano
Nesta parte do laboratório, vai utilizar um microscópio para observar o movimento browniano no pó vermelho carmim, que é um corante obtido a partir das vísceras pulverizadas de fêmeas de escaravelhos cochonilhas.
Materiais
- Lâmina de vidro
- Palito de dente
- Pó vermelho carmim
- Folha de cobertura
- Água da torneira
Procedimento
- Pegue numa lâmina de microscópio e coloque nela uma gota de água da torneira.
- Com um palito, adicionar cuidadosamente uma quantidade muito pequena de pó vermelho carmim à gota de água e colocar uma lamela.
- Observar com varrimento, baixa e depois alta potência.
Perguntas de laboratório
- Descreva a atividade das partículas de vermelho carmim na água.
- Se a lâmina fosse aquecida, a velocidade de movimento das moléculas aceleraria, abrandaria ou permaneceria a mesma? Porquê?
Parte 2: Difusão através de uma Membrana Semipermeável
Devido à sua estrutura, a membrana celular é uma membrana semipermeável, o que significa que ALGUMAS substâncias podem facilmente difundir-se através dela, como o oxigénio ou o dióxido de carbono. Outras substâncias, como a glicose ou os iões de sódio, não conseguem atravessar a membrana celular, a não ser que sejam especificamente transportadas através de proteínas incorporadas na própria membrana. Se uma substância é ou não capaz de se difundir através deNeste laboratório, vamos fazer "células" de tubos de diálise e explorar o efeito de tamanho na capacidade de uma molécula se difundir através de uma "membrana celular".
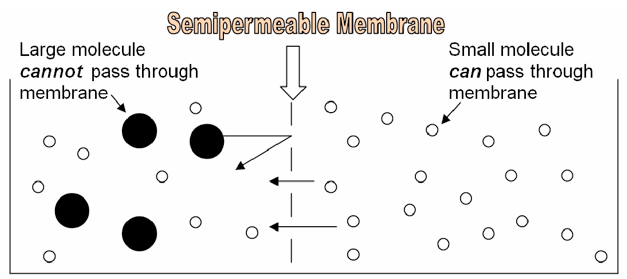
As informações seguintes podem ser úteis para compreender e interpretar os resultados obtidos neste laboratório:
- Fenolftaleína
- Fórmula atómica: C 20 H 14 O 4
- Massa atómica: 318,32 g/mol
- Cor em solução ácida : Límpido
- Cor da solução básica: Rosa
- Iodo
- Fórmula atómica: I ou I2
- Materiais
- Massa atómica: 126 g/mol
- Amido
- Fórmula atómica: (C 6 H 10 O 5 )n
- Massa atómica: ENORME!
- Cor em iodo: Azulado
- Hidróxido de sódio
- Fórmula atómica: NaOH
- Massa atómica: 40,1 g/mol
- Ácido/base: Base
Materiais
- 2 peças de tubo de diálise
- Linha
- Fenolftaleína
- Iodo
- Lápis de cera
- 2 copos
- NaOH
- Solução de amido
- Pipetador
- Pipeta
Procedimento
- Utilizando um lápis de cera, identifique um copo #1 e o outro copo #2.
- Encher o copo 1 com 300 ml de água da torneira e adicionar 10 gotas de NaOH 1 M. Não derramar o NaOH - é muito cáustico!
- Encher o copo n.º 2 com 300 ml de água da torneira e adicionar gotas de iodo, gota a gota, até a solução ficar amarela brilhante.
- Feche uma extremidade de cada tubo de diálise dobrando cuidadosamente a extremidade "estilo cachorro-quente" 2 vezes e depois "estilo hambúrguer" 1 vez. Amarre a parte dobrada do tubo firmemente com um fio. É fundamental que o tubo esteja bem fechado para evitar fugas.
- Adicionar 10 ml de água e três gotas de fenolftaleína a um dos sacos de tubos de diálise. Fechar a outra extremidade do saco dobrando e atando cuidadosamente como anteriormente.
- Lavar bem o saco que contém a fenolftaleína e colocá-lo no copo que contém o NaOH.
- Adicionar 10 ml de solução de amido ao outro tubo de diálise. Voltar a fechar bem o saco e enxaguar como acima indicado. Colocar este saco com a solução de amido no copo n.º 2.
- Deixar que a difusão ocorra entre os sacos e as soluções nos copos.
- Após 10 minutos, observe as mudanças de cor nos dois sacos e nas soluções externas. Faça um desenho de cada sistema abaixo.
Dados
Registar as cores (em baixo) e etiquetar o conteúdo dentro e fora dos sacos (em cima):
| Copo 1 | Copo 2 | |||
|---|---|---|---|---|
| Inicial | Final | Inicial | Final | |
| Cor do interior do saco | ||||
| Saco exterior a cores (no copo) | ||||
Perguntas de laboratório
- Qual a substância que se difundiu através da membrana no copo 1? Como é que sabe?
- Qual a substância que se difundiu através da membrana no copo n.º 2? Como é que sabe?
- Porque é que alguns iões e moléculas podem passar através do saco de diálise e outros não?
Parte 3: Osmose e a membrana celular
A osmose é o movimento da água através de uma membrana semipermeável (como a membrana celular). A tonicidade de uma solução envolve a comparação da concentração do citoplasma de uma célula com a concentração do seu ambiente. Em última análise, a tonicidade de uma solução pode ser determinada examinando o efeito que uma solução tem numa célula dentro da solução.
Por definição, uma solução hipertónica é uma solução que provoca a contração de uma célula. Embora seja certamente mais complexa do que isto, para os nossos objectivos nesta aula, podemos assumir que uma solução hipertónica é mais concentrado Se uma célula encolhe quando colocada numa solução, então a solução é hipertónico para a célula.
Se uma solução for hipotónica para uma célula, então a célula inchará quando colocada na solução hipotónica. Neste caso, pode imaginar que a solução é menos concentrado do que o citoplasma da célula, fazendo com que a água da solução flua em a célula. A célula incha!
Por fim, uma solução isotónica é aquela que não causa qualquer alteração na célula. Pode imaginar que a solução e a célula têm concentrações iguais, pelo que não há movimento líquido de moléculas de água para dentro ou para fora da célula.
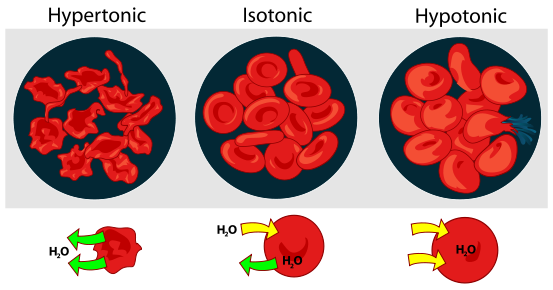
Neste exercício, vai observar a osmose expondo uma célula vegetal à água salgada.
Previsão
O que achas que vai acontecer à célula neste ambiente? Faz um desenho da tua hipótese.
Materiais
- Folha de Elodea
- Lâmina de microscópio
- Folha de cobertura
- Solução de NaCl a 5%
Procedimento
- Retirar uma folha de uma planta Elodea com a pinça.
- Faça uma montagem húmida da folha. Utilize a água do lago para fazer a montagem húmida.
- Observa as células de Elodea ao microscópio composto em alta resolução (400 X) e desenha uma célula típica.
- Em seguida, adicione várias gotas de solução salina a 5% ao bordo da lamela para permitir que o sal se difunda sob a lamela. Observe o que acontece às células (pode ser necessário procurar ao longo dos bordos da folha). Procure células que tenham sido visivelmente alteradas.
Resultados
Desenha uma célula típica, tanto em água salgada como em água de lago, e identifica a membrana celular e a parede celular.
Perguntas de laboratório
- O que é que vê acontecer à membrana celular quando a célula foi exposta à água salgada? Porque é que isso acontece?
- Descreva os termos hipertónico, hipotónico e isotónico.
- Como é que as suas observações se alterariam se o NaCl pudesse passar facilmente através da membrana celular e entrar na célula?
Parte 4: Conceção experimental
Tu e o teu grupo irão planear uma experiência para determinar os pesos moleculares relativos do azul de metileno e do permanganato de potássio. Poderás utilizar uma placa de Petri com ágar, que é um meio semelhante a uma gelatina, feito a partir de um polissacárido que se encontra nas paredes celulares das algas vermelhas. Terás também acesso a uma broca de cortiça e a uma pequena régua de plástico.
Materiais
- 1 placa de Petri com ágar
- Azul de metileno
- Permanganato de potássio
- Outro?
Conceção
O projeto da experiência deve incluir todas as partes seguintes:
- Hipótese
- Conceção experimental
- Dados
- Conclusões
- Outras questões/outros comentários